天津?qū)DI的要求?
日期:2022-01-04 來源: 點擊:
天津市是率先開展醫(yī)療器械唯一標識全域試點的城市。
根據(jù)國家藥監(jiān)局、國家衛(wèi)生健康委《醫(yī)療器械唯一標識系統(tǒng)試點工作方案》的統(tǒng)一部署,天津市藥監(jiān)局和醫(yī)保局、衛(wèi)生健康委在2020年5月25日聯(lián)合印發(fā)《天津市醫(yī)療器械唯一標識系統(tǒng)試點工作方案》,正式開啟天津市UDI試點工作。
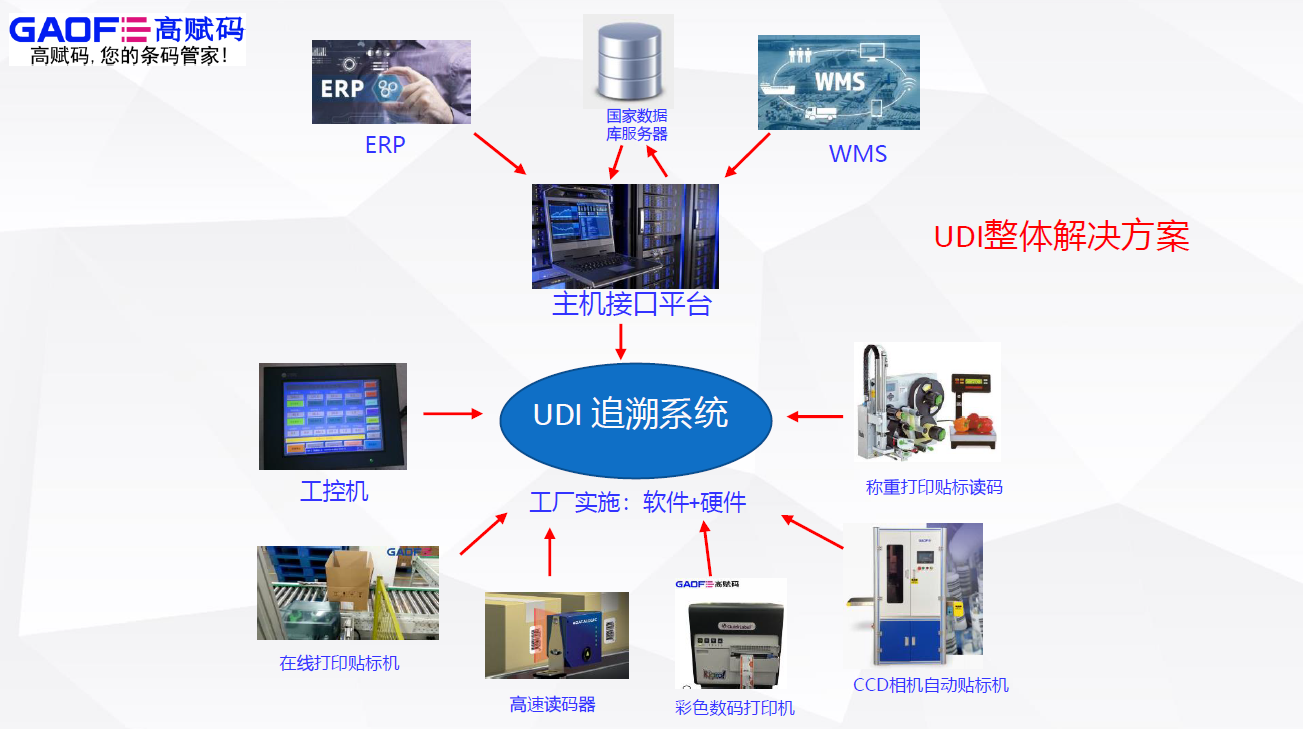
第一批參與試點的醫(yī)療器械注冊人16家、經(jīng)營企業(yè)2家、使用單位3家。開展此項工作旨在建立系統(tǒng)框架。構(gòu)建醫(yī)療器械唯一標識系統(tǒng),涵蓋醫(yī)療器械唯一標識的創(chuàng)建、賦予以及數(shù)據(jù)上傳下載和共享等功能,建設(shè)天津市醫(yī)療器械唯一標識數(shù)據(jù)平臺,實現(xiàn)與國家藥品監(jiān)督管理局醫(yī)療器械唯一標識數(shù)據(jù)庫的有效對接和醫(yī)用物資大數(shù)據(jù)平臺的基本構(gòu)建。2020年6月30日,天津市藥監(jiān)局如期完成第一批試點工作,形成生產(chǎn)企業(yè)申報賦碼上傳、經(jīng)營企業(yè)掃碼使用、使用單位掃碼入庫的基本格局。
2020年10月30日,天津市藥監(jiān)局、醫(yī)保局、衛(wèi)生健康委又聯(lián)合印發(fā)《關(guān)于聯(lián)合開展天津市醫(yī)療器械唯一標識系統(tǒng)全域試點工作的通知》,在全國率先開展UDI全域試點,將天津市第三類、第二類醫(yī)療器械產(chǎn)品和京津冀醫(yī)用耗材聯(lián)合采購平臺范圍內(nèi)進口及其他省市生產(chǎn)的品種納入試點范圍,要求醫(yī)療器械生產(chǎn)企業(yè)實現(xiàn)賦碼上傳;醫(yī)療器械經(jīng)營企業(yè)實現(xiàn)有碼盡掃;二級以上公立醫(yī)療機構(gòu)實現(xiàn)掃碼應(yīng)用,開創(chuàng)了UDI試點“三醫(yī)聯(lián)動”新局面。
同時,構(gòu)建追溯體系,探索建立覆蓋生產(chǎn)、經(jīng)營、使用等各環(huán)節(jié)的醫(yī)療器械全生命周期的追溯管理體系,對醫(yī)療器械產(chǎn)品追溯標準化體系進行科學(xué)研究,將研究成果作為政策出臺、職責(zé)分工、平臺建設(shè)、進度安排等工作實施的重要參考依據(jù)。對接醫(yī)療管理,探索醫(yī)療器械唯一標識在衛(wèi)健、醫(yī)保等領(lǐng)域的銜接應(yīng)用,與國家醫(yī)保高值醫(yī)用耗材編碼形成映射,使醫(yī)療器械唯一標識系統(tǒng)與高值醫(yī)用耗材采購和醫(yī)保支付審核平臺完成對接,建立共同參與、共創(chuàng)價值、共享成果的良性機制,實現(xiàn)醫(yī)療器械審評審批、臨床應(yīng)用、日常監(jiān)管、醫(yī)保結(jié)算等信息平臺的數(shù)據(jù)共享。